No todos nos levantamos y saltamos de la cama listos para el día. Algunos, como yo, necesitamos un poco de energía extra para salir del sueño y entrar en el día. Cuando me tomo una taza de café, mi nivel de energía se dispara y estoy bien para el resto del día. Las reacciones químicas funcionan de forma muy parecida. También necesitan su café. Lo llamamos energía de activación.
Entender cómo funciona esto puede ser una perspectiva útil como parte de nuestra construcción de modelos mentales.
Tanto si utilizas la química en tu trabajo diario como si has hecho lo posible por no pensar en ella desde la escuela, las ideas que subyacen a la energía de activación son sencillas y útiles fuera de la química. Entender el principio puede, por ejemplo, ayudarte a conseguir que los niños se coman las verduras, a motivarte a ti mismo y a los demás, y a superar la inercia.
Cómo funciona la energía de activación en química
Las reacciones químicas necesitan una determinada cantidad de energía para empezar a funcionar. La energía de activación es la energía mínima necesaria para que se produzca una reacción.
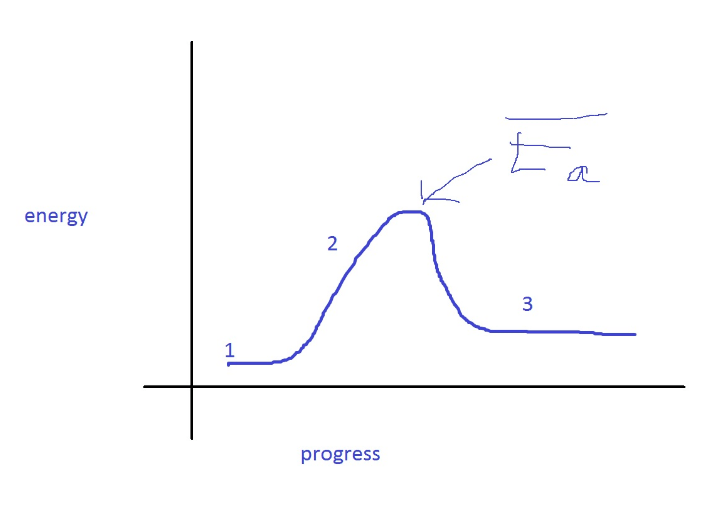
Para entender la energía de activación, debemos pensar primero en cómo se produce una reacción química.
Cualquiera que haya encendido alguna vez un fuego tendrá una comprensión intuitiva del proceso, aunque no lo haya relacionado con la química.
La mayoría de nosotros tenemos una idea general del calor necesario para iniciar las llamas. Sabemos que poner una sola cerilla en un tronco grande no será suficiente y que un lanzallamas sería excesivo. También sabemos que los materiales húmedos o densos requerirán más calor que los secos. La cantidad imprecisa de energía que sabemos que necesitamos para iniciar un fuego es representativa de la energía de activación.
Para que se produzca una reacción, deben romperse los enlaces existentes y formarse otros nuevos. Una reacción sólo se producirá si los productos son más estables que los reactivos. En un incendio, convertimos el carbono en forma de madera en CO2 y es una forma de carbono más estable que la madera, por lo que la reacción procede y en el proceso produce calor. En este ejemplo, la energía de activación es el calor inicial necesario para que se inicie el fuego. Nuestro esfuerzo y las cerillas gastadas son representativos de esto.
Podemos pensar en la energía de activación como la barrera entre los mínimos (valores mínimos necesarios) de los reactivos y los productos en una reacción química.
La ecuación de Arrhenius
Svante Arrhenius, científico sueco, estableció la existencia de la energía de activación en 1889.
Arrhenius desarrolló su ecuación homónima para describir la correlación entre la temperatura y la velocidad de reacción.
La ecuación de Arrhenius es crucial para calcular la velocidad de las reacciones químicas y, sobre todo, la cantidad de energía necesaria para iniciarlas.
En la ecuación de Arrhenius, K es el coeficiente de velocidad de reacción (la velocidad de reacción). A es el factor de frecuencia (la frecuencia con la que chocan las moléculas), R es la constante universal de los gases (unidades de energía por incremento de temperatura por mol), T representa la temperatura absoluta (normalmente medida en kelvins) y E es la energía de activación.
No es necesario conocer el valor de A para calcular Ea, ya que se puede averiguar a partir de la variación de los coeficientes de velocidad de reacción en función de la temperatura. Como muchas ecuaciones, puede reordenarse para calcular diferentes valores. La ecuación de Arrhenius se utiliza en muchas ramas de la química.
Por qué importa la energía de activación
Comprender la energía necesaria para que se produzca una reacción nos permite controlar nuestro entorno.
Volviendo al ejemplo del fuego, nuestro conocimiento intuitivo de la energía de activación nos mantiene a salvo. Muchas reacciones químicas tienen elevados requisitos de energía de activación, por lo que no proceden sin un aporte adicional. Todos sabemos que un libro sobre un escritorio es inflamable, pero no arderá sin la aplicación de calor. A temperatura ambiente, no tenemos que ver el libro como un peligro de incendio. Si encendemos una vela sobre el escritorio, sabemos que debemos alejar el libro.
Si las reacciones químicas no tuvieran requisitos fiables de energía de activación, viviríamos en un mundo peligroso.
Catalizadores
Las reacciones químicas que requieren cantidades importantes de energía pueden ser difíciles de controlar.
Aumentar la temperatura no siempre es una fuente de energía viable debido a los costes, los problemas de seguridad o la simple inviabilidad. Las reacciones químicas que se producen dentro de nuestro cuerpo, por ejemplo, no pueden utilizar altas temperaturas como fuente de energía de activación. En consecuencia, a veces es necesario reducir la energía de activación necesaria.
Acelerar una reacción reduciendo la energía de activación necesaria se llama catalización. Esto se hace con una sustancia adicional conocida como catalizador, que generalmente no se consume en la reacción. En principio, sólo se necesita una pequeña cantidad de catalizador para provocar la catálisis.
Los catalizadores funcionan proporcionando una vía alternativa con menores requisitos de energía de activación. En consecuencia, un mayor número de partículas tiene energía suficiente para reaccionar. Los catalizadores se utilizan en las reacciones a escala industrial para reducir los costes.
Volviendo al ejemplo del fuego, sabemos que intentar encender un gran tronco con una cerilla rara vez es eficaz. Añadir un poco de papel proporcionará una vía alternativa y servirá de catalizador; los encendedores hacen lo mismo.
Dentro de nuestro cuerpo, las enzimas sirven como catalizadores en reacciones vitales (como la construcción del ADN).
“La energía puede tener dos dimensiones. Una es la de la motivación, la de ir a alguna parte, la de la meta, este momento es sólo un medio y la meta va a ser la dimensión de la actividad, orientada a la meta; entonces todo es un medio, de alguna manera hay que hacerlo y hay que llegar a la meta, entonces te relajarás. Pero para este tipo de energía, la meta nunca llega, porque este tipo de energía sigue cambiando cada momento presente en un medio para otra cosa, en el futuro. La meta siempre permanece en el horizonte. Sigues corriendo, pero la distancia sigue siendo la misma.
No, hay otra dimensión de la energía: esa dimensión es la celebración inmotivada. La meta está aquí, ahora; la meta no está en otro lugar. De hecho, tú eres la meta. De hecho, no hay más realización que la de este momento: considera los lirios. Cuando tú eres la meta y cuando la meta no está en el futuro, cuando no hay nada que conseguir, sino que simplemente la celebras, entonces ya la has conseguido, está ahí. Esto es relajación, energía desmotivada”.– Osho, Tantra
Aplicar el concepto de energía de activación a nuestra vida cotidiana
Aunque la energía de activación es un concepto científico, podemos utilizarlo como modelo mental práctico.
Volviendo al ejemplo del café de la mañana, muchas de las cosas que hacemos cada día dependen de un impulso inicial.
Pongamos el ejemplo de una clase de estudiantes que se propone hacer una redacción para su curso. Cada alumno necesita un tipo de energía de activación diferente para ponerse en marcha. Para un alumno, podría ser escuchar a su amiga decir que ya ha terminado la suya. Para otro, podría ser bloquear las redes sociales y apagar su teléfono. Otro estudiante podría necesitar unas cuantas latas de Red Bull y un plazo de entrega inminente. O, para otro, leer un artículo interesante sobre el tema que le proporcione una chispa de inspiración. El acto de escribir una redacción requiere un cierto tipo de energía.
Conseguir que los niños coman sus verduras puede ser un proceso difícil. En este caso, los incentivos pueden actuar como catalizadores. “No puedes tomar el postre hasta que no te comas las verduras” no sólo es un juego psicológico de incentivos, sino que además suele requerir menos energía que pelearse constantemente con los niños para que se coman las verduras. Una vez que los niños se comen una zanahoria, generalmente se comen otra y otra. Aunque sigan queriendo el postre, no tendrás que recordárselo cada vez, por lo que ahorrarás mucha energía.
El concepto de energía de activación también puede aplicarse a la realización de cambios drásticos en la vida. Cualquiera que haya hecho alguna vez algo drástico y difícil (como dejar una adicción, abandonar una relación abusiva, dejar un trabajo de larga duración o hacer cambios cruciales en el estilo de vida) sabe que es necesario llegar primero a un punto de ruptura. Cuanto más grande y desafiante es una acción, más energía de activación necesitamos para realizarla.
Nuestro bebedor de café puede necesitar poca energía de activación (una o dos tazas) para empezar su día si está bien descansado. En cambio, necesitará mucho más café para ponerse en marcha si ha dormido mal y tiene un día aburrido que superar.
Conclusión
Para entender y utilizar el concepto de energía de activación en nuestras vidas no hace falta ser licenciado en química. Aunque el concepto tal y como lo utilizan los científicos es complejo, podemos utilizar la idea básica.
No es casualidad que muchos de los más útiles modelos mentales de nuestro entramado tengan su origen en la ciencia. Hay algo bastante poético en la forma en que el comportamiento humano refleja lo que ocurre a nivel microscópico.
Si quieres ver otros ejemplos, fíjate en la Navaja de Occam, la falsificación, los bucles de retroalimentación y el equilibrio.






